氟和氟盐是化工原料。由于氟气性质活泼 很晚才制取出来。(1)不能通过电解纯净的液态HF获得F2 其原
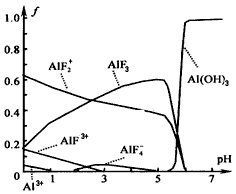
| 氟和氟盐是化工原料。由于氟气性质活泼,很晚才制取出来。 (1)不能通过电解纯净的液态HF获得F2,其原因是_________________;但电解液态KHF2时,两极分别得到F2和H2,写出阳极上HF2-放电产生气体的电极反应式__________________ (2)利用化学反应也能制取氟。请配平下列化学方程式 ①____K2MnF6+____SbF5→KSbF6+____MnF3+____F2↑; ②其中还原产物是__________ (3)某温度下测得浓度均为0.10 mol/L 的KF和HF混合溶液的pH=4,近似计算HF的电离平衡常数Ka(写出计算过程)。 (4)一定浓度的HF和Al2(SO4)3混合液中,铝的各种微粒含量f随pH的分布曲线如图示。用NaOH使混合液的pH从5调整到7,写出有关反应的离子方程式:______________________ |
 |
参考解答
| (1)氟化氢是共价化合物,纯液态时不电离,因而不导电;HF2--2e-=F2↑+H+ (2)①2 4 4 2 1;②MnF3 |
(3)解: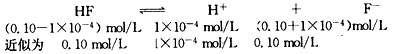 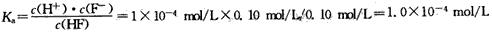 |
| (4)AlF2++3OH-=Al(OH)3↓+2F-;AlF3+ 3OH-=Al(OH)3↓+3F- |
相似问题
有下列三个反应:①Cl2+FeI2FeCl2+I2 ②2Fe2++Br22Fe3++2Br-③Co2
有下列三个反应:①Cl2+FeI2FeCl2+I2 ②2Fe2++Br22Fe3++2Br-③Co2O3+6HCl2CoCl2+Cl2↑+3H2O,下列说法中正确的是( )A.①②③中氧化产物分别是FeCl2、F
实验室可用KMnO4固体和浓盐酸反应制氯气 反应的化学方程式如下:2KMnO4+16HCl(浓)2K
实验室可用KMnO4固体和浓盐酸反应制氯气,反应的化学方程式如下:2KMnO4+16HCl(浓)2KCl+2MnCl2+5Cl2↑+8H2O。(1)该反应中氧化剂是_____________,还原
有A B C D四种金属片 进行如下实验:①A B用导线相连后 同时浸入稀H2SO4溶液中 A极为负
有A、B、C、D四种金属片,进行如下实验:①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;②C、D用导线连接后浸入稀H2SO4中,电流由D导线C;③A
下列反应中水既不是氧化剂 又不是还原剂的氧化还原反应是[ ]A.SO3 + H2O = H2
下列反应中水既不是氧化剂,又不是还原剂的氧化还原反应是[ ]A.SO3 + H2O = H2SO4 B.2Na2O2 +2H2O = 4NaOH + O2↑ C.2F2+2H2O = 4HF+O2 D.NaH+H2O = NaOH + H2↑
海洋是资源的宝库 蕴藏着丰富的化学元素 如氯 溴 碘 镁等。按要求回答下列问题:(1)可以证明溴比碘
海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘、镁等。按要求回答下列问题:(1)可以证明溴比碘的氧化性强的离子反应方程式为________________












