如图一为NaCl KNO3的溶解度曲线.(1)20℃时 NaCl的溶解度是______.(2)20℃
如图一为NaCl、KNO3的溶解度曲线.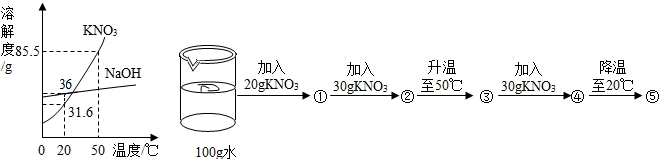 (1)20℃时,NaCl的溶解度是______. (2)20℃时,将20gNaCl固体投入到50g水中,得到的是NaCl的______(填“饱和”或“不饱和”)溶液,此时溶液中溶质的质量分数是______(保留到0.1%). (3)除去KNO3固体中混有的少量NaCl,提纯的步骤是:加水溶解、蒸发浓缩、______,然后过滤、洗涤、干燥. (4)某同学在20℃时进行了如图二实验,得到相应的溶液①~⑤,下列说法正确的是______ A.向④加入4.5gKNO3即可达到饱和B.②③⑤中溶质的质量分数相等 C.①③④均为KNO3的不饱和溶液D.④→⑤可析出53.9gKNO3晶体. |
参考解答
| (1)由溶解度曲线图可知20℃时,NaCl的溶解度是36g; (2)20℃时,NaCl的溶解度是36g,即该温度下,100g水中最多溶解36g氯化钠,所以50g水中最多溶解18g,所以20℃时,将20gNaCl固体投入到50g水中,得到的是NaCl的饱和溶液,此时溶液中溶质的质量分数是:
(3)硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受温度影响较小,所以利用降温结晶方法进行分离,具体方法是:加水溶解、蒸发浓缩,降温结晶,过滤、洗涤、干燥. (4)在20℃时进行了如下实验,则:①已知在20℃时硝酸钾的溶解度为31.6克,则20克硝酸钾全部溶解;②又加入的30克硝酸钾只能溶解11.6克;③加热知50℃时,50克硝酸钾全部溶解;④再加30克硝酸钾,全部溶解,因为在50℃时,其溶解度为85.5克;⑤降温至20℃时,由晶体析出,只能溶解31.6克 A、由以上知,④中的溶质为80g,在50℃时,其硝酸钾溶解度为85.5克,所以应在加5.5克,达到饱和,故A错误; B、②中溶质为31.6g,③中的溶质是50g,⑤中的溶质是31.6g,所以②③⑤中溶质的质量分数不相等,故B错误; C、由以上分析知,①③④均为不饱和溶液;故C正确; D、④→⑤可析出的晶体为:80-31.6=48.4g,故D错误; 故选C. 故答案为:(1)36.0g;(2)饱和;26.5%;(3)降温结晶;(4)C. |
相似问题
下图是A B C三种固体物质的溶解度曲线.t1℃时 将25gA B C三种固体分别加入100g水中.
下图是A,B,C三种固体物质的溶解度曲线.t1℃时,将25gA,B,C三种固体分别加入100g水中.则:(1)t1℃时,所得三种物质的溶液中为不饱溶液的是______
如图为A B两种固体物质的溶解度曲线.请回答:(1)曲线上Q点表示______.(2)在l0℃时 两
如图为A、B两种固体物质的溶解度曲线.请回答:(1)曲线上Q点表示______.(2)在l0℃时,两种物质的饱和溶液中溶质的质量分数A______B(选填“>”、“
如图为A B C三种物质的溶解度曲线 请据图判断下列叙述中不正确的是( )A.t1℃时 B物质的溶
如图为A,B,C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )A.t1℃时,B物质的溶解度为40gB.t2℃时,三种物质的溶解度由大到小的顺序
右图是甲 乙两物质的溶解度曲线 以下说法正确的是( )A.t1℃时甲 乙两物质的溶解度均为30gB
右图是甲、乙两物质的溶解度曲线,以下说法正确的是( )A.t1℃时甲、乙两物质的溶解度均为30gB.甲物质的溶解度大于乙物质的溶解度C.甲、乙两物质
某温度下 某物质的溶解度为25克 则该溶质的饱和溶液中溶质 溶剂 溶液的质量之比为( )A.1:2
某温度下,某物质的溶解度为25克,则该溶质的饱和溶液中溶质、溶剂、溶液的质量之比为( )A.1:2:3B.1:4:5C.5:3:2D.2:3:4












