(10分)某市热电厂使用的燃料是含硫较多的煤.该厂附近一所中学的同学经常闻到空气有异味 且空气能见度
| (10分)某市热电厂使用的燃料是含硫较多的煤.该厂附近一所中学的同学经常闻到空气有异味,且空气能见度差.学习化学后,同学们意识到这有可能是该厂排出的废气超标造成的,于是在老师的指导下做了探究实验,请你填写下列空白, 【提出问题】该厂附近所降雨水是否是酸雨?空气里SO2是否超标呢? 【查阅资料】I.我国关于SO2在风景区、居民区、工厂区的空气质量最高标准分别见下表: 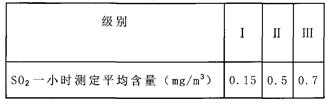 Ⅱ.硫酸钡既不溶于水,也不溶于酸(如不与稀盐酸、稀硝酸等反应). 【设计实验1】第一组同学取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示: 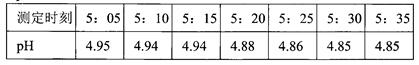 所降雨水 (填“是”或“不是”)酸雨。在测定时间内酸雨pH减小的原因可能是__ 【设计实验2】第二小组同学设计以下步骤来测定空气中SO2的含量. (1)用2L的空可乐瓶采集工厂附近的空气样品,采样的具体操作是: (2)向取回的装有空气样品的可乐瓶中倒入NaOH溶液,盖紧瓶塞后充分振荡,仿照CO2与NaOH溶液的反应,写出SO2与NaOH溶液反应的化学方程式: (3)加入一定量氧化剂H2O2,使其中Na2SO3完全转化为Na2SO4.向可乐瓶中加入过量的BaCl2溶液.Na2SO4和BaCl2反应的化学方程式为: ____ (4)经过过滤、洗涤、烘干,称量固体质量为1.165mg. 计算:1.165mg硫酸钡中硫元素的质量为 mg.由质量守恒定律可知,2L空气样品中SO2的质量为 mg. 由空气质量标准可得出结论:该厂排放的SO2严重超标.。 【发现新问题】考虑到空气中的各种气体成分,第一组认为第二组同学的SO2的含量偏大,其依据是 ;你提出的实验改进方案是 【反思与应用】为尽快改善该地区的空气质量,请你提出一条合理化建议: |
参考解答
| 是,随时间的延长亚硫酸逐渐氧化为硫酸;【设计实验2】(1)可任瓶装满水盖上盖拿到工厂附近,倒掉水,再盖上瓶盖;(2)2NaOH + SO2 ='===' Na2SO3 + H2O;(3)Na2SO4+BaCl2==BaSO4↓+2NaCl;(4)0.16;0.32;【发现新问题】空气中的二氧化碳也能与氢氧化钠溶液反应,反应后生成的碳酸钠要与氯化钡溶液反应,生成碳酸钡沉淀;向沉淀中加入过量的稀硝酸后在进行其他操作;【反思与应用】减少化石燃料的使用;工厂的废水处理达标后在排放等. |
试题分析:【设计实验1】pH<5.6的雨水属于酸雨,故所降雨水是酸雨,在测定时间内酸雨pH减小的原因可能是随时间的延长亚硫酸逐渐氧化为硫酸;【设计实验2】(1)用2L的空可乐瓶采集工厂附近的空气样品,采样的具体操作是可任瓶装满水盖上盖拿到工厂附近,倒掉水,再盖上瓶盖;(2)SO2与NaOH溶液反应的化学方程式:2NaOH + SO2 ='===' Na2SO3 + H2O;(3)Na2SO4和BaCl2反应的化学方程式为Na2SO4+BaCl2==BaSO4↓+2NaCl;(4)1.165mg硫酸钡中硫元素的质量为1.165mg× 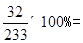 0.16mg; 2L空气样品中SO2的质量为0.32mg【发现新问题】考虑到空气中的各种气体成分,第一组认为第二组同学的SO2的含量偏大,其依据是空气中的二氧化碳也能与氢氧化钠溶液反应,反应后生成的碳酸钠要与氯化钡溶液反应,生成碳酸钡沉淀;向沉淀中加入过量的稀硝酸后在进行其他操作; 【反思与应用】为尽快改善该地区的空气质量,提出合理化建议:减少化石燃料的使用;工厂的废水处理达标后在排放等. 0.16mg; 2L空气样品中SO2的质量为0.32mg【发现新问题】考虑到空气中的各种气体成分,第一组认为第二组同学的SO2的含量偏大,其依据是空气中的二氧化碳也能与氢氧化钠溶液反应,反应后生成的碳酸钠要与氯化钡溶液反应,生成碳酸钡沉淀;向沉淀中加入过量的稀硝酸后在进行其他操作; 【反思与应用】为尽快改善该地区的空气质量,提出合理化建议:减少化石燃料的使用;工厂的废水处理达标后在排放等. |
相似问题
(8分) “侯氏制碱法”制得的纯碱(Na2CO3)中常含有少量氯化钠。某化学兴趣小组的同学拟测定某纯
(8分) “侯氏制碱法”制得的纯碱(Na2CO3)中常含有少量氯化钠。某化学兴趣小组的同学拟测定某纯碱样品中Na2CO3的质量分数。【方案一】沉淀分析法(如下图
(8分)金属在生产 生活中有着广泛的应用。(1)铝在空气中具有很好的抗腐蚀性能 原因是(用化学方程式
(8分)金属在生产、生活中有着广泛的应用。(1)铝在空气中具有很好的抗腐蚀性能,原因是(用化学方程式表示)(2)春节期间,小明妈妈从市场买了一匹金
下图是某粒子X的结构示意图 下列叙述正确的是 A.该粒子第一电子层有7个电子B.该粒子核内有17个质
下图是某粒子X的结构示意图,下列叙述正确的是 A.该粒子第一电子层有7个电子B.该粒子核内有17个质子C.该粒子在化学反应中容易失去电子D.该粒子与铝
金属加工后的废切削液中含有2~5%的NaNO2 它是一种环境污染物。人们用NH4Cl溶液来处理此废切
金属加工后的废切削液中含有2~5%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理此废切削液,使NaNO2转化为无毒物质。该反应分两步进行:第一步:Na
(7分)(1) 请用化学用语填空:①2个氢分子 ②氯化亚铁中的阳离子
(7分)(1) 请用化学用语填空:①2个氢分子 ②氯化亚铁中的阳离子③最简单的有机物 ④配制波尔多液时用的盐(2)写出下列反应的化学方程式:①硫在












