在400℃ 101kPa时 NO2(g)+CO(g)?NO(g)+CO2(g)反应过程的能量变化如图
| 在400℃、101kPa时,NO2(g)+CO(g)?NO(g)+CO2(g)反应过程的能量变化如图所示. (1)该反应是______(填“吸热”或“放热”)反应. (2)该反应的热化学方程式为______. (3)改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的是______. a.浓度 b.压强 c.温度 d.催化剂. 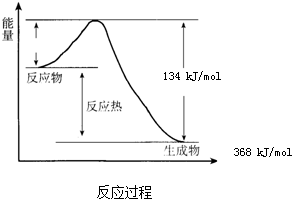 |
参考解答
| (1)因反应物的能量高于生成物的能量时,反应是放热反应,故答案为:放热; (2)由图知没反应放出的热量为368KJ?mol-1-134KJ?mol-1=234KJ?mol-1,且该反应为放热反应,热化学方程式为NO2(g)+CO(g)?NO(g)+CO2(g)△H=-234KJ?mol-1, 故答案为:NO2(g)+CO(g)?NO(g)+CO2(g)△H=-234KJ?mol-1; (3)催化剂能降低活化能,加快反应速率,故答案为:d. |
相似问题
已知25℃ 101kpa条件下:(1)4Al(s)+3O2(g)═2Al2O3(s);△H=-283
已知25℃、101kpa条件下:(1)4Al(s)+3O2(g)═2Al2O3(s);△H=-2834 9kJ?mol-1(2)4Al(s)+2O3(g)═2Al2O3(s);△H=-3119 1KJ?mol-1由此得
下列物质加入水中显著放热的是[ ]A.生石灰 B.固体NaCl C.无水乙醇
下列物质加入水中显著放热的是[ ]A.生石灰B.固体NaCl C.无水乙醇D.固体NH4NO3
下列说法中正确的是[ ]A.在化学反应过程中 发生物质变化的同时不一定发生能量变化B.生成物
下列说法中正确的是[ ]A.在化学反应过程中,发生物质变化的同时不一定发生能量变化B.生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所
化学反应一定伴随能量变化.(1)将20gBa(OH)2?8H2O晶体与10g NH4Cl晶体一起放入
化学反应一定伴随能量变化.(1)将20gBa(OH)2?8H2O晶体与10gNH4Cl晶体一起放入烧杯中,并将烧杯放在滴有几滴水的玻璃片上,用玻璃棒快速搅拌,闻到___
反应物的总能量低于生成物的总能量的反应是( )A.Na2O2和CO2的反应B.Al和盐酸的反应C.
反应物的总能量低于生成物的总能量的反应是( )A.Na2O2和CO2的反应B.Al和盐酸的反应C.Mg在O2中燃烧D.Ba(OH)2?8H2O与NH4Cl固体的反应












