Ⅰ 氮元素是重要的非金属元素 可形成卤化物 氮化物 叠氮化物及配合物等多种化合物。(1)NF3 NB
| Ⅰ、氮元素是重要的非金属元素,可形成卤化物、氮化物,叠氮化物及配合物等多种化合物。 (1)NF3,NBr3、NCl3这三种分子的空间构型是 。 (2)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-。请写出两种与N3-电子数相等的分子 。 (3)NaN3与KN3离子键强弱相比,NaN3 KN3(填“>”、“=”或“<” )。 (4)氮化碳结构如下图, 其硬度超过金刚石晶体,成为首屈一指的超硬新材料。  ①写出氮化碳的化学式____ _ _____; ②指出氮化碳的晶体类型______ _____。 Ⅱ、分析表中四种物质的相关数  据,请回答: 据,请回答:
(2)NH3和PH3比较,分  解温度高低的原因是_____ ______; 解温度高低的原因是_____ ______;(3)结合上述数据和规律判  断,一定压强下HF和HCl的混合气体降温时___________先液化。 断,一定压强下HF和HCl的混合气体降温时___________先液化。 |
参考解答
| I (1)三角锥型 (2) 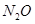 或 或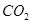 (3)> (4)① 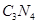 ②原子晶体 ②原子晶体II (1)结构相似时,相对分子质量越大,分子间作用力越大,因此 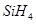 沸点高于 沸点高于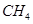 (2)氮的废金属性比磷强,所以氮比磷比氢稳定。(3)HF |
| 略 |
相似问题
下列说法中正确的是( )A.NO2 SO2 BF3 NCl3分子中没有一个分子中原子的最外层电子都
下列说法中正确的是( )A.NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构B.P4和CH4都是正四面体形分子且键角都为10
(8分)【化学-物质结构与性质】碳族元素包括:C Si Ge Sn Pb。(1)碳纳米管有单层或
(8分)【化学-物质结构与性质】碳族元素包括:C、Si、 Ge、 Sn、Pb。(1)碳纳米管有单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过
某些化学键的键能如下表所示(kJ·mol-1):键H-HBr-BrI-ICl-ClH-ClH-IH-
某些化学键的键能如下表所示(kJ·mol-1):键H-HBr-BrI-ICl-ClH-ClH-IH-Br键能436193151247431299356(1)把1mol Cl2分解为气态原子时,需要__
(4分)下面是你熟悉的物质:①O2② 金刚石 ③ NaBr ④ H2SO4⑤ Na2CO3⑥ K2S
(4分)下面是你熟悉的物质:①O2② 金刚石 ③ NaBr ④ H2SO4⑤ Na2CO3⑥ K2S⑦NaHSO4小题1:这些物质中,只含共价键的是_______________;只含离
(8分)在有机溶剂里若m跟m定量地发生完全反应 生成 同时得到一种白色固体R。R的熔点为113℃ 在
(8分)在有机溶剂里若m跟m定量地发生完全反应,生成,同时得到一种白色固体R。R的熔点为113℃,在减压下50℃即可升华,测得R的蒸气密度为折算成标准状况












