有A B C D E五种短周期元素 它们的原子序数依次增大 已知A和B原子有相同的电子层数 且A的最
| 有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,已知A和B原子有相同的电子层数,且A的最外层电子数是次外层电子数的两倍,C是该周期中原子半径最大的元素,C的单质在高温下与B的单质充分反应,可以得到与D单质颜色相同的固态化合物C2B2,E与D相邻. 试根据以上叙述回答: (1)元素名称 C______ E______ (2)写出物质的电子式 AB2______ C2B______ (3)用电子式表示CE的形成过程______ (4)D、E的气态氢化物的稳定性______>______(填化学式) (5)写出C、E两种元素的最高价氧化物对应的水化物间反应的离子方程式______. |
参考解答
| A和B原子有相同的电子层数,则二者位于相同周期,且A的最外层电子数是次外层电子数的两倍,则A应为C元素,C是该周期中原子半径最大的元素,应为Na元素,C的单质在高温下与B的单质充分反应,可以得到与D单质颜色相同的固态化合物C2B2,则该化合物为Na2O2,为黄色固体,则B为O元素,D为S元素,E与D相邻,且有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,则E为Cl元素, (1)由以上分析可知:C为Na元素,E为Cl元素,故答案为:Na;Cl; (2)AB2为CO2,为共价化合物,电子式为 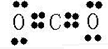 ,C2B为Na2O,为离子化合物,电子式为 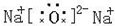 ,故答案为: 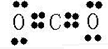 ; 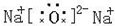 ; (3)CE为NaCl,用电子式表示形成过程为:  , 故答案为:  ; (4)D、E的气态氢化物的分别为H2S、HCl,元素的非金属性越强,则对应的氢化物越稳定,则有HCl>H2S, 故答案为:HCl;H2S; (5)C、E两种元素的最高价氧化物对应的水化物分别为NaOH和HClO4,二者反应的离子方程式为:OH-+H+=H2O, 故答案为:OH-+H+=H2O. |
相似问题
金属钛对人体无毒且惰性 能与肌肉和骨骼生长在一起 有“生物金属”之称.下列有关 4822Ti和 50
金属钛对人体无毒且惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称.下列有关4822Ti和5022Ti的说法中正确的是( )A.4822Ti和5022Ti原子中均含
A B C D E五种短周期元素 其原子序数依次增大 而原子半径按A C B E D顺序依次增大.A
A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D顺序依次增大.A、D同主族;B、D、E三种元素原子的最外层电子数之和为10;
aXn-和 bYm+为两种主族元素的离子 它们的核外电子排布相同 下列判断中正确的是( )A.原子
aXn-和bYm+为两种主族元素的离子,它们的核外电子排布相同,下列判断中正确的是( )A.原子序数:X>YB.a-n=b+mC.离子半径:Xn->Ym+D.原子半径:X>Y
A.B均为原子序数1-20的元素 已知A的原子序数为n A2+离子比B2-离子少8个电子 则B的原子
A.B均为原子序数1-20的元素,已知A的原子序数为n,A2+离子比B2-离子少8个电子,则B的原子序数是( )A.n+4B.n+6C.n+8D.n+10
短周期元素A B C的原子序数依次递增 其原子的最外层电子数之和为9 A与C同主族 B原子最内层电子
短周期元素A、B、C的原子序数依次递增,其原子的最外层电子数之和为9,A与C同主族,B原子最内层电子数为最外层电子数的2倍,下列有关叙述正确的是(












