过渡金属元素氧化物的应用研究是目前科学研究的前沿之一。2007年诺贝尔物理学奖为法国科学家阿尔贝·费
过渡金属元素氧化物的应用研究是目前科学研究的前沿之一。2007年诺贝尔物理学奖为法国科学家阿尔贝·费尔和德国科学家彼得·格林贝格尔共同获得,以表彰他们在巨磁电阻效应(CMR效应)研究方面的成就。某钙钛型复合氧化物(如下图),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应。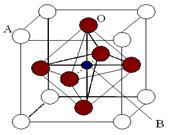 (1)用A、B、O(氧)表示此类特殊晶体的化学式 ; (2)已知La为+3价,当被钙等二价元素A替代时,可形成复合钙钛矿化合物La1-xAxMnO3, (x < 0.1),此时一部分锰转变为+4价。导致材料在某一温度附近有反铁磁-铁磁、铁磁-顺磁转变及金属-半导体的转变,则La1-xAxMnO3中三价锰与四价锰的物质的量之比为 ;(用含x的代数式表示) (3)Mn的外围电子排布式为 ,在元素周期表中的位置是第 周期,第 族; (4)下列有关说法正确的是 。 A.镧、锰、氧分别位于周期表f、d、p区 B.CaO的熔点为2614℃,属于原子晶体 C.铬的堆积方式与钾相同,则其堆积方式如下图: 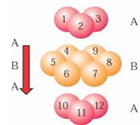 D.锰的电负性为1.59 ,Cr的电负性为1.66,说明锰的金属性比铬强 |
参考解答
| (1)ABO3(2分) (2)(1-x)/x (2分) (3)3d54s2 (2分) 四(1分) ⅦB(1分) (4)AD (2分) |
试题分析:(1)每个面心是2个晶胞所共用,顶点是8个晶胞所共用,故用A、B、O(氧)表示此类特殊晶体的化学式ABO3。 (2)假设三价锰的物质的量为a, 四价锰的物质的量为b,根据化学式化合价代数和为0可知: [(3a+4b)/(a+b)+3-3x+2x-6=0 解得:a/b=(1-x)/x。 (3)Mn的原子序数是25,属于过度元素,在元素周期表中的位置是第四周期,第ⅦB族,外围电子排布式为3d54s2。 (4)B项:CaO是由离子组成的离子化合物,属于离子晶体,故错;C项:图因为  ,故错。故选AD。 ,故错。故选AD。点评:本题考查的是晶体的相关知识,题目难度较大,需要学生平时多加练习这方面的知识。 |
相似问题
现有下列七种物质 根据要求填空:A 液氧 B KCl C 冰水混合物 D 氖 E 干冰
现有下列七种物质,根据要求填空:A液氧 B KCl C冰水混合物 D氖 E干冰 F Na2CO3 G食盐水(1)直接由原子构成的物质是(填编号,下同);(2)只由分
下列说法正确的是(NA为阿伏加德罗常数的值( )A.124g P4含有的P-P键的个数为4NAB
下列说法正确的是(NA为阿伏加德罗常数的值( )A.124g P4含有的P-P键的个数为4NAB.12 g石墨中含有C-C键的个数为2NAC.12g金刚石中含有C-C键的个数为2N
下列各项中 理由 结论及因果关系均正确的是选项理由结论A键能:N≡N>Cl-Cl单质沸点:N2>Cl
下列各项中,理由、结论及因果关系均正确的是选项理由结论A键能:N≡N>Cl-Cl单质沸点:N2>Cl2B分子中可电离的H+个数:H2SO4>CH3COOH酸性:H2SO4>CH3
如图示意的是硼和镁形成的化合物的晶体结构单元;镁原子间形成正六棱柱 且棱柱的上下底面还各有一个镁原子
如图示意的是硼和镁形成的化合物的晶体结构单元;镁原子间形成正六棱柱,且棱柱的上下底面还各有一个镁原子,6个硼原子位于棱柱内。则该化合物的化学式可
美国LawreceLiremore国家实验室(LLNL)的V.Lota.C.S.Yoo和Cynn成功
美国LawreceLiremore国家实验室(LLNL)的V Lota C S Yoo和Cynn成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2的原子晶体说法中正确的












