0.2mol 有机物和 0.4mol O2在密闭容器中燃烧后的产物为 CO2 CO 和 H2O(g)
| 0.2mol 有机物和 0.4mol O2在密闭容器中燃烧后的产物为 CO2、CO 和 H2O(g)。 燃烧后的这些产物经过浓H2SO4后,质量增加 10.8g;再通过灼热的 CuO 充分反 应后,固体质量减轻 3.2g,最后气体再通过碱石灰被完全吸收,质量增加 17.6g。 (1)推断该有机物的分子式。 (2)若 0.2mol 该有机物在与过量的金属钠完全反应后放出 4.48LH2(标准状 况),试确 定有机物的结构简式。 |
参考解答
(1)C2H6O2 (2) 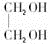 |
| ①浓H2SO4增重说明生成水的质量为10.8 g。②灼热的CuO减重3.2 g,说明生成CO的量,而CO又被氧化为CO2,故碱石灰增重实际为原燃烧生成的CO2及CO被氧化生成的CO2质量之和。 ③该物质与金属钠能发生反应产生H2,说明含有—OH,这是推断其结构的依据。 ④O2的量不足量。 根据条件: (1)燃烧产物中有CO,说明有机物燃烧时O2不足。CO通过灼热的CuO充分反应后,CuO质量减轻3.2 g,即参与反应的CuO中含氧元素3.2 g,也就是有机物燃烧时减少的O2的质量为3.2 g。 3.2 g O2的物质的量为 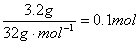 ,即有机物完全燃烧时需O2的物质的量为:0.4 mol+0.5 mol ='0.9' mol;有机物完全燃烧后生成CO2和水的物质的量为:n(CO2)= ,即有机物完全燃烧时需O2的物质的量为:0.4 mol+0.5 mol ='0.9' mol;有机物完全燃烧后生成CO2和水的物质的量为:n(CO2)= 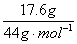 ='0.4' mol n(H2O)= ='0.4' mol n(H2O)=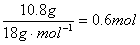 设该有机物的分子式为CxHyOz。  该有机物的分子式为C2H6O2。 (2)可与Na反应放出H2,说明其结构中含有羟基(—OH)。 n(H2)= 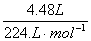 ='0.2' mol ='0.2' molC2H6O2 ~ H2 0.2 mol 0.2 mol 1 mol 1 mol 1 mol C2H6O2与Na反应后可放出1 mol H2,说明C2H6O2分子中含有2个可被Na置换的氢原子,即含有2个—OH,为C2H4(OH)2,结构简式为 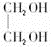 。 。 |
相似问题
(11分)有机物A是烃的含氧衍生物。在同温同压下 A蒸气的质量是同体积乙醇蒸气的2倍。1.38 g的
(11分)有机物A是烃的含氧衍生物。在同温同压下,A蒸气的质量是同体积乙醇蒸气的2倍。1 38 g的A完全燃烧后,将燃烧产物通过碱石灰,碱石灰增重3 06 g;
下列说法中 正确的是( )A.金属钠可保存在无水乙醇中B.含碳原子较少的低级醇无毒C.乙醇和乙醚
下列说法中,正确的是()A.金属钠可保存在无水乙醇中B.含碳原子较少的低级醇无毒C.乙醇和乙醚互为同分异构体D.乙醇是可再生的无污染能源
(10分)将乙醇和汽油按一定比例混配作为燃料 可缓解能源供应紧张的矛盾。请回答下列问题:(1)写出由
(10分)将乙醇和汽油按一定比例混配作为燃料,可缓解能源供应紧张的矛盾。请回答下列问题:(1)写出由“纤维素→葡萄糖→乙醇”中的由“纤维素→葡萄糖”
近几年一种新型的甜味剂木糖醇悄悄地走人生活 进入人们的视野 因为木糖醇是一种理想的蔗糖代替 品 它具
近几年一种新型的甜味剂木糖醇悄悄地走人生活,进入人们的视野,因为木糖醇是一种理想的蔗糖代替 品,它具有甜味足,溶解性好,防龋齿,适合糖尿病患者
(10分)α-松油醇可经以下路线合成 小方框中的每一字母各代表一种有机物:可供选择的试剂:①Br2
(10分)α-松油醇可经以下路线合成,小方框中的每一字母各代表一种有机物:可供选择的试剂:①Br2②H2③O2请回答下列问题:(1)试剂1是___________,试












