过量液态汞加到1.00×10-3mol.dm-3酸化了的Fe3+溶液中 假定只有下面反应发生:2Hg
过量液态汞加到1.00×10-3mol.dm-3酸化了的Fe3+溶液中,假定只有下面反应发生:2Hg+2Fe3+→Hg22++2Fe2+,在25℃达平衡时,只留下4.6%Fe3+,试计算Eθ(H22+/Hg)。(已知Eθ(Fe3+/Fe2+)=0.770 V)
请帮忙给出正确答案和分析,谢谢!
参考解答
正确答案: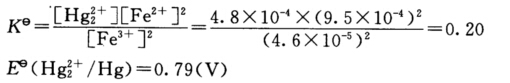
相似问题
计算pH=3.0 [HF]+[F-]=0.10(mol.dm-3)时 Fe3+/Fe2+的电对的Eθ
计算pH=3.0,[HF]+[F-]=0.10(mol dm-3)时,Fe3+/Fe2+的电对的Eθ。请帮忙给出正确答案和分析,谢谢!
把碱金属离子通过一阳离子交换树脂 它们被吸附的顺序为________________。请帮忙给出正确
把碱金属离子通过一阳离子交换树脂,它们被吸附的顺序为________________。请帮忙给出正确答案和分析,谢谢!
00 cm30.500 0 mol.dm-3Ce4+溶液使10.00 cm31.600 mol.dm
00 cm30.500 0 mol dm-3Ce4+溶液使10.00 cm31.600 mol dm-3 Sn2+刚好完全氧化成Sn4+,那么Ce在还原产物中的氧化态是什么?请帮忙给出正确答案和分析,谢谢!
取一小块金属钠 用滤纸吸干表面的煤油 放入盛有少量汞的研钵中 小心研磨得液态钠汞合金(以NaHg表示
取一小块金属钠,用滤纸吸干表面的煤油,放入盛有少量汞的研钵中,小心研磨得液态钠汞合金(以NaHg表示),均分成两份。把一份放入试管中加入少量水,搅拌
称取2.200 g KHC2O4.H2C2O4.2H2O配制于250.mL容量瓶中 移取25.00
称取2.200 g KHC2O4 H2C2O4 2H2O配制于250.mL容量瓶中,移取25.00 mL,用NaOH滴定消耗24.00 mL;移取25.00 mL,于酸性介质中用KMnO4滴定消耗30












